Fundamentos
A Termodinâmica é o estudo do fluxo de energia entre corpos. A Termodinâmica Clássica (TC) apoia-se em quatro leis fundamentais, que foram desenvolvidas a partir da metade do século XIX pelos trabalhos de diversos cientistas notáveis, como Clausius, Thomson, Carnot, Boltzmann, Gibbs, Helmholtz entre outros. Para entender quais são as regras que determinam como a energia é transferida entre corpos, precisamos, primeiramente, definir o que é um sistema termodinâmico, o que é energia, e como ela pode ser adicionada ou removida de sistemas.
Sistemas e subsistemas
Um sistema é uma região do universo na qual estamos interessados. O seu tamanho varia, de acordo com o nosso interesse. Ele pode corresponder a um copo de água ou até uma piscina olímpica. Pode ser composto por apenas uma substância, como água, ou por uma mistura de diferentes substâncias, como o ar atmosférico. Também pode ser constituído por apenas uma fase – isto é, possuir os mesmos valores de propriedades macroscópicas, como a densidade, ao longo de toda a sua extensão –, como uma barra de cobre puro, ou possuir diversas fases, como um copo de água com gelo. Para a termodinâmica, a capacidade de o sistema trocar matéria e/ou energia também é fundamental para a descrição de problemas físico-químicos.
Desta forma, chamamos de sistema aberto um sistema que pode trocar matéria e energia, como a água dentro da panela que é aquecida no fogão. Um sistema é denominado fechado caso ele só possa trocar energia, mas não matéria, com outros corpos - uma garrafa de refrigerante fechada, por exemplo. Por fim, sistemas são chamados de isolados caso eles não possam trocar nem matéria nem energia com outros corpos, como uma garrafa térmica de café.
O sistema é uma região delimitada do espaço e essa separação pode ser feita por uma barreira física real, como as paredes de um copo, ou por uma fronteira imaginária, que definimos segundo critérios convenientes ao estudo. Para além das fronteiras do sistema, o restante constitui a vizinhança. Por exemplo, caso estejamos interessados em descrever como a energia é transferida para dentro ou para fora de um copo de água, o sistema será composto pela água do copo e todo o resto será a vizinhança. O conjunto sistema e vizinhança formam o universo.
No geral, iremos estudar o fluxo de energia entre o sistema e a vizinhança. Caso o sistema esteja fisicamente separado da vizinhança, então a barreira divisória entre eles pode ser de dois tipos: paredes diatérmicas, que permitem a passagem de calor (a ser definido) entre vizinhança e sistema, e paredes adiabáticas, que não permitem a troca de calor e matéria entre as partes.
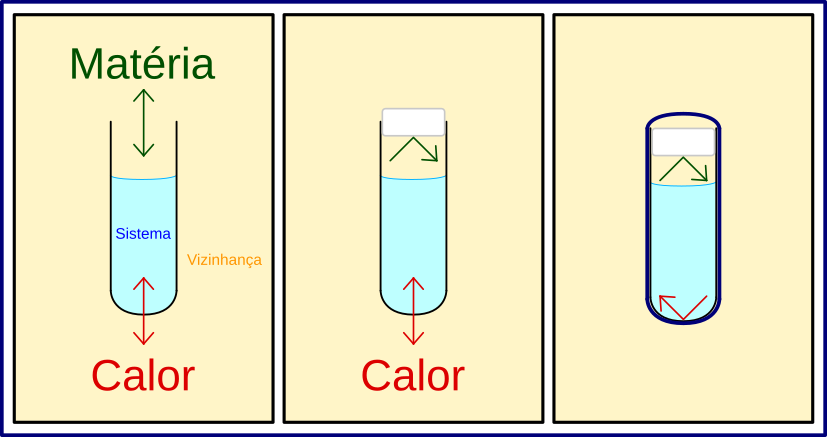
Figura 1. Três tipos de sistemas termodinâmicos. Esquerda) Sistema aberto, matéria pode ser inserida/removida do sistema e processos de calor podem ocorrer; Meio) Sistema fechado, pode haver processos de calor, mas matéria não pode ser inserida/removida do sistema; Direita) Sistema isolado por meio de uma barreira adiabática, matéria não pode ser inserida/removida e não é possível haver processos de calor.
Para além do fluxo de energia entre vizinhança e sistema, por vezes será útil separar o sistema em partes menores, que chamamos de subsistemas. A separação entre os subsistemas pode ser física ou imaginária, também, e o conjunto de todos os subsistemas forma o próprio sistema.
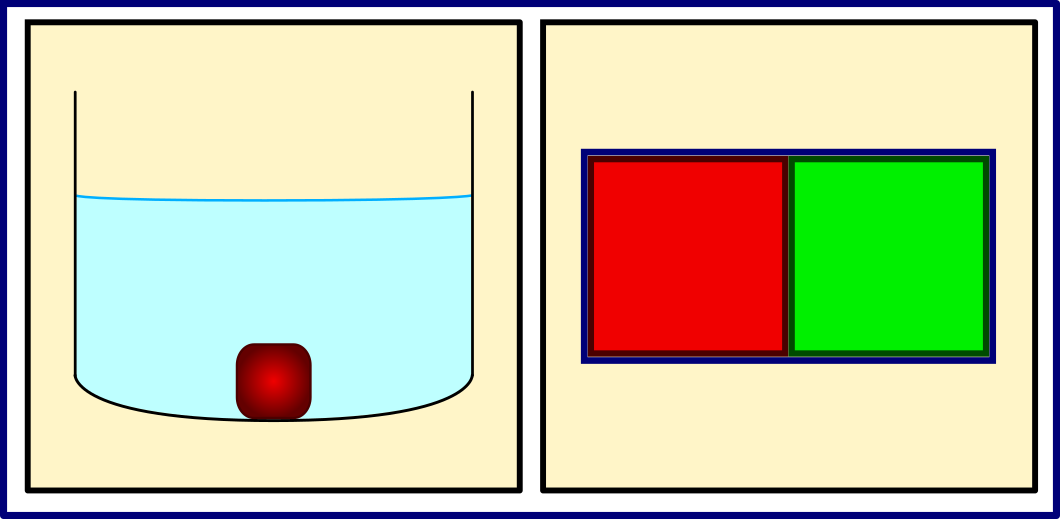
Figura 2. Dois tipos de sistemas: Esquerda) Sistema composto por água e bloco de metal aquecido, bifásico; Direita) Dois subsistemas inicialmente em estados distintos, separados por paredes diatérmicas, mas isolados do resto do universo.
Estado termodinâmico de um sistema
A entrada e saída de energia de um sistema ocorrem através de processos (calor e trabalho, como veremos). Esses eventos, no geral, fazem com que as propriedades dos sistemas variem. Então, é fundamental que consigamos definir como um dado sistema se encontra antes e depois de uma transformação. Para isso, utilizamos o conceito de estado termodinâmico de um sistema. Definimos por estado termodinâmico o conjunto de variáveis macroscópicas suficientes para caracterizar um sistema. Por exemplo, para um gás ideal, o conjunto das variáveis pressão (p), volume (V) e temperatura (T) pode ser utilizado para caracterizar o estado do sistema.
Assim, se dois cientistas, em lugares diferentes do mundo, trabalham com o mesmo gás ideal, nas mesmas condições de pressão, volume e temperatura, então estes gases se encontram no mesmo estado termodinâmico. O conjunto de todas as variáveis macroscópicas necessárias para definir o estado do sistema é conhecido por conjunto completo.
Precisamos ressaltar que na termodinâmica clássica que descreveremos aqui, serão tratados apenas sistemas que se encontram no equilíbrio termodinâmico, isto é, sistemas cujas propriedades macroscópicas não variam ao longo do tempo. Isso significa que a evolução temporal do sistema ao longo de uma transformação não será tratada aqui - isto é assunto para outro ramo da termodinâmica, que trata de sistemas fora do equilíbrio. Assim, nossos os sistemas estudados aqui estarão em equilíbrio, no início e no final de processos.
Propriedades extensivas $vs$ propriedades intensivas
Todas as propriedades termodinâmicas podem ser classificadas em dois grupos: elas são ou intensivas ou extensivas. Propriedades intensivas são propriedades que dependem do tamanho do sistema. Vamos considerar um sistema homogêneo, que possui uma certa propriedade $\alpha_T$. Essa grandeza física pode ser pressão, energia, densidade, capacidade térmica, ou qualquer outra grandeza característica que pertença ao sistema. Agora, vamos subdividir esse sistema em dezesseis subsistemas menores, por exemplo. Vamos utilizar barreiras imaginárias para isso, e definir que cada subsistema possuirá a sua propriedade $\alpha_i$, com $i=1, \cdots, 16,$ conforme a Figura 3.
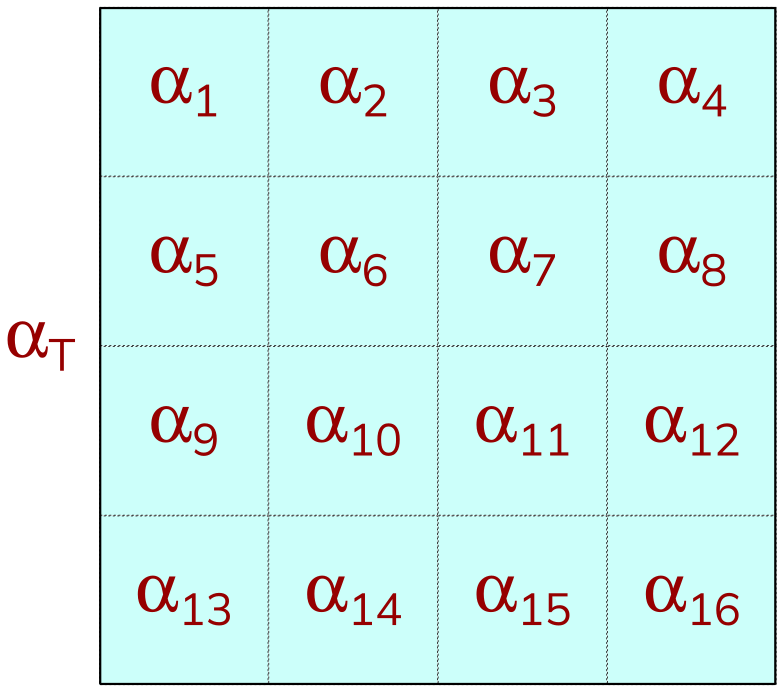
Figura 3. Um sistema subdividido em dezesseis subsistemas. $\alpha_T$ é a propriedade do sistema como um todo e e cada subsistema possui um $\alpha_i$, com $i=1, \cdots, 16$.
Agora, podemos imaginar dois cenários. No primeiro, podemos dizer que:
isto é, que a grandeza como um todo é a soma das partes. Denominamos esse tipo de grandeza de extensiva, isto é, que depende do tamanho do sistema. Diversas propriedades físico-químicas são desse tipo, como por exemplo a massa, o volume, a energia interna, a energia de Gibbs, a entropia, as capacidades térmicas, entre tantas.
No segundo cenário, podemos definir:
ou seja, que a propriedade $\alpha$ é a mesma para o sistema como um todo, não importando o tamanho do sistema, ou subdivisões. Esse tipo de grandeza é chamada de intensiva. Exemplos de propriedades desse tipo são a temperatura, a densidade, a energia interna molar, a entropia molar, a capacidade térmica específica, e várias outras.
Por fim, notemos que a divisão de uma grandeza extensiva por outra grandeza extensiva dá origem a uma grandeza intensiva ($\rho = \frac{m}{V}; \bar U = \frac{U}{n}; C_s = \frac{C}{m}$; etc).
Com as definições acima, podemos começar a discutir propriedades de sistemas físico-químicos.