A Lei Zero da Termodinâmica foi definida depois das três leis mais famosas da termodinâmica. Contudo, por ser uma lei mais fundamental que elas, foi chamada de Lei Zero. Talvez ela tenha sido definida mais tarde por ser uma lei intuitiva, que parecia carecer de fundamentação matemática - que apresentaremos uma versão abaixo.
A temperatura
A temperatura é uma propriedade, de certa forma, única. Todos nós temos uma idéia intuitiva do que ela é, mas pode ser difícil definí-la exatamente. Podemos relacioná-la com a energia cinética, como na equação TC2.4. Mas, mesmo sem uma equação para atribuir significado físico, podemos sentir diferenças de temperatura constantemente. Apesar de não conseguirmos dizer seu valor exato (em qualquer unidade que se escolha), ao tocarmos simultaneamente em dois corpos distintos, sabemos dizer qual deles está mais quente.
Definindo o equilíbrio térmico
Isso quer dizer que sentimos quando os dois corpos possuem a mesma temperatura - ou possuem valores muito próximos. Vamos considerar um sistema composto de dois subsistemas (1 e 2), compostos por gases (1 e 2, respectivamente). Ambos estão em contato entre si, através de uma barreira inicialmente adiabática fixa, e ambos estão isolados da vizinhança. Vamos considerar, também, que a temperatura do subsistema ($\theta_1$) 1 é diferente da temperatura do subsistema 2 ($\theta_2$).
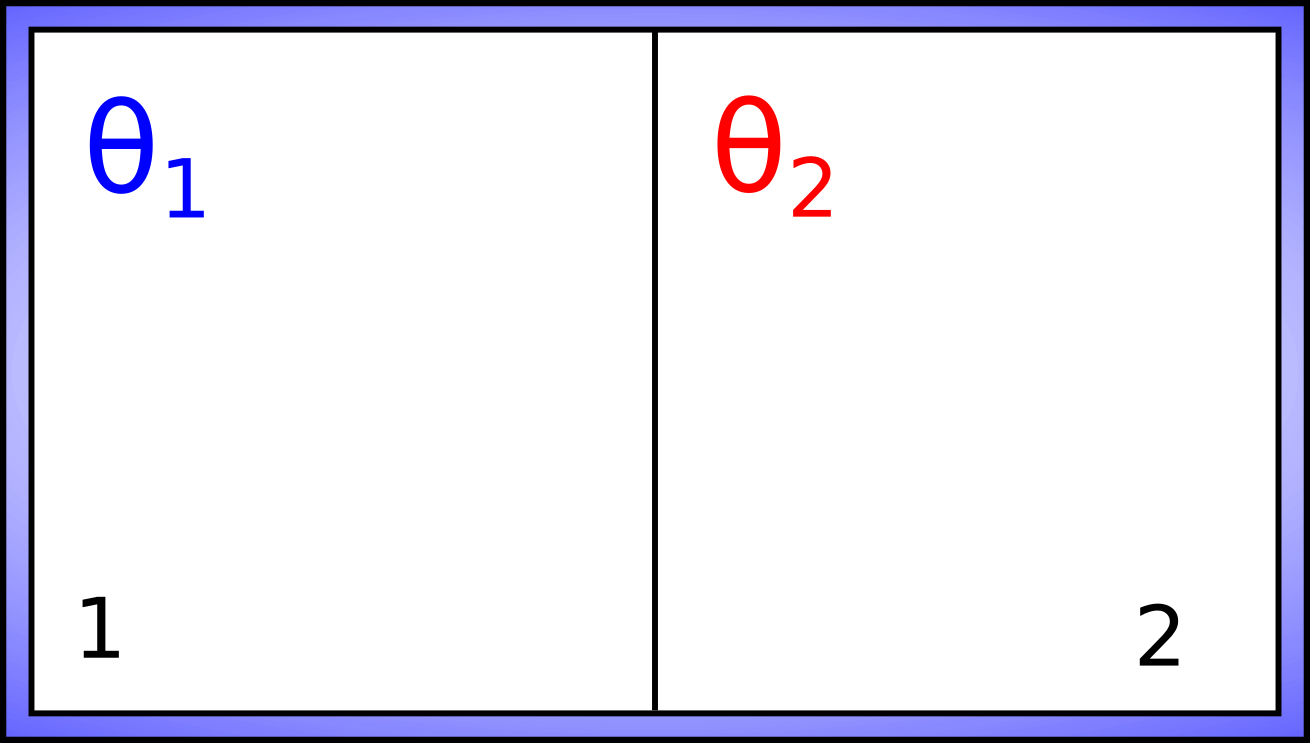
Intuitivamente, sabemos que este sistema se encontra fora do equilíbrio térmico - definido aqui de forma sensorial e intuitiva. Como as paredes são adiabáticas, não haverá calor (processo a ser definido, ainda) e ambos permanecerão como estão. Vimos que gases possuem equações de estado e que elas são relações matemáticas entre propriedades macroscópicas do sistema. Vamos considerar a equação abaixo:
com $i = 1, 2$, e sendo $p_i$, $\rho_i$ e $\$theta_i$ a pressão, densidade e temperatura do subsistema $i$, respectivamente. Utilizamos $\rho$ aqui para que a equação não dependa de propriedades extensivas. Agora, vamos assumir que podemos separar as variáveis do sistema e escrever uma função só da temperatura, $\theta$, e uma função de $p$ e $\rho$:
e, enquanto a parede separando os dois subsistemas for adiabática, então os sistemas não se encontram no equilíbrio térmico e $g (\color{blue}{\theta_1}\color{black}) \ne g (\color{red}{\theta_2}\color{black})$. Logo, podemos dizer, também, que $\varphi (p_1,\rho_1) \ne \varphi (p_2,\rho_2)$.
Matematicamente
Agora, vamos transformar a parede adiabática entre os dois subsistemas em diatérmica, fixa e rígida. Intuitivamente, sabemos que haverá calor, e o subsistema com maior $\theta$ transferirá energia para o subsistema com menor $\theta$, até que a temperatura de ambos seja igual. Quando isso ocorrer, teremos $g (\textcolor{blue}{\theta_1}) = g (\textcolor{red}{\theta_2})$ e diremos que os dois subsistemas estão em equilíbrio térmico. Agora, vamos imaginar um terceiro subsistema, 3, em contato com o primeiro, mas não com o segundo. Caso ele esteja em equilíbrio com o primeiro, então $g (\textcolor{blue}{\theta_1}) = g (\textcolor{green}{\theta_3})$.
Daí, concluímos que:
Enunciado da Lei Zero
Podemos, então, enunciar a Lei Zero da Termodinâmica:
"Dois sistemas, cada um separadamente em equilíbrio térmico com um terceiro, estão em equilíbrio térmico entre si."