Desvio de idealidade em gases
Como discutido anteriormente, gases ideais não existem – alguns gases reais se comportam idealmente, dependendo das condições experimentais. Isso decorre do fato de moléculas ocuparem um volume no espaço (não são puntiformes) e poderem realizar interações intermoleculares. Apesar disso, é possível determinar equações de estado para gases reais – isto é, é possível escrever equações que relacionem as variáveis do conjunto completo (V, p, n, T) para esses gases. Na verdade, diversas equações já foram desenvolvidas para tal finalidade, através de diferentes metodologias e para atingir propósitos variados. Veremos abaixo algumas delas.
O fator de compressibilidade, Z
A pergunta inicial é: como podemos quantificar desvios de idealidade de um gás? Uma forma prática de se fazer isso é definindo o fator de compressibilidade, Z:
sendo $M$ a massa molar da molécula, $\rho$ a densidade mássica do sistema e $\bar V$ é o volume molar do gás, definido como . Ao longo do curso, a barra sobre uma propriedade sempre denotará uma propriedade molar - a não ser que especificado de outra forma. E notamos que, para um gás ideal, $Z = 1$ para toda e qualquer combinação possível de valores de pressão, volume, número de mols e temperatura, i.e., o produto da pressão pelo volume será sempre igual ao produto de número de mols, temperatura e constante dos gases ideais.
Nem mesmo para gases nobres o estado do gás pode ser calculado (em todas as condições) pela equação dos gases ideais. Por exemplo, observamos desvios de idealidade para argônio, um gás nobre (Figura 1).
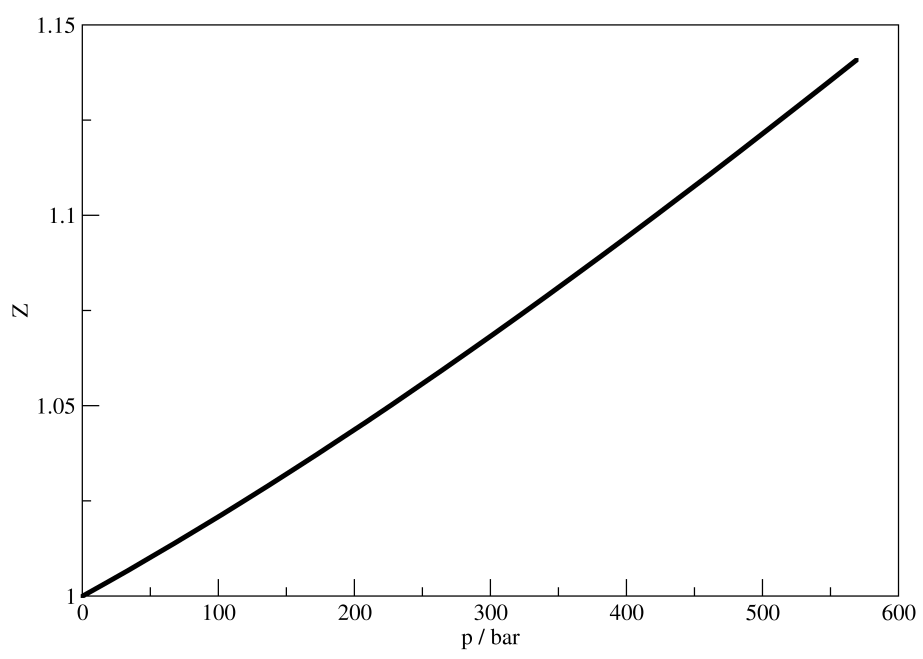
Figura 1. Fator de compressibilidade do argônio, a 800 K, em função da pressão do sistema.
Gases reais ou imperfeitos
Como esperado, $Z = 1$ para pressões baixas. Contudo, notamos que há desvio de idealidade, pois $Z \neq 1$ em pressões mais elevadas – $Z$ aumenta de forma quase linear com a pressão. Quando um gás não se comporta idealmente, dizemos que o gás é um gás real ou gás imperfeito, naquelas condições. O fator de compressibilidade de argônio, a 800 K, aumenta com a pressão de forma quase linear no intervalo de pressão apresentado. Esse aumento, contudo, é relativamente pequeno, chegando a $Z \approx 1,15$. Isso ocorre pois as interações intermoleculares de Ar são fracas quando comparadas a de outras moléculas, e devemos esperar desvios mais consideráveis e não-lineares (até mesmo, perfis não-monotônicos) nesses casos. Por exemplo, o perfil do fator de compressibilidade para o N2O em diferentes temperaturas é apresentado abaixo (Figura 2):
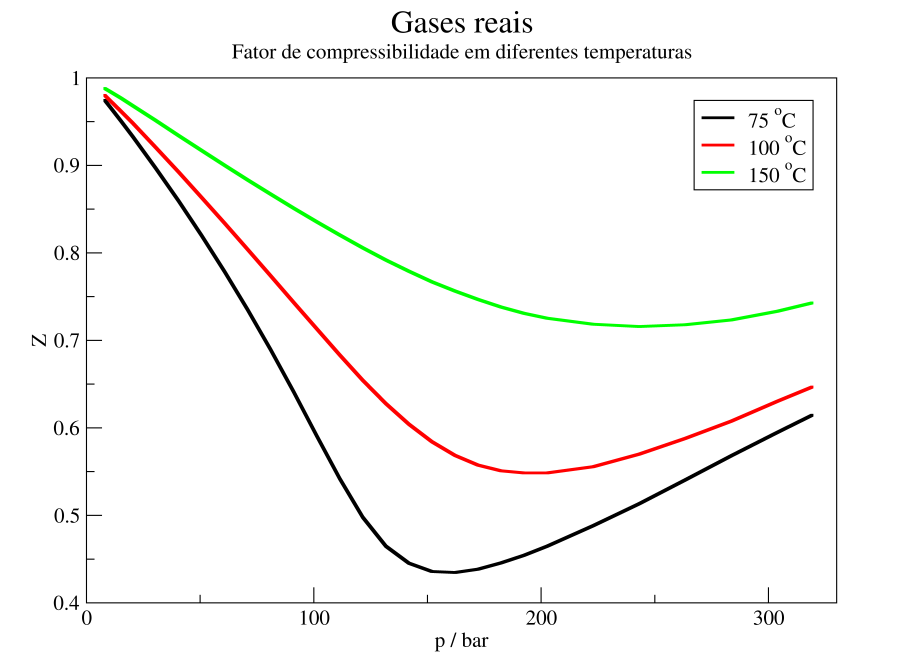
Figura 2. Fator de compressibilidade de N2O gasoso em função da pressão, para diferentes temperaturas. Valores plotados foram obtidos a partir do trabalho de Couch & Kobe.1
Vemos que o fator de compressibilidade, independente da temperatura reportada, desvia da idealidade ( $Z = 1$) para uma grande faixa de valores de pressão. Neste caso específico, o desvio é dito negativo, pois os valores de $Z$ são menores do que a unidade. Além disso, vemos que o aumento da temperatura faz com que os desvios sejam menores, isto é, as curvas se aproxima do ideal conforme a temperatura aumenta – sem nunca se igualarem a 1. Apesar de serem diferentes, as três curvas possuem uma mesma característica: todas se aproximam da unidade no limite em que a pressão tende a zero. Na verdade, isso é observado para todos os gases, independente da natureza deles. De forma análoga, podemos escrever o fator de compressibilidade em função do inverso do volume molar e, neste caso, veríamos que $Z$ tende a 1 quando o volume molar tende ao infinito. Por fim, se analisarmos o comportamento de $Z$ com a densidade, veremos que $Z$ tende a 1 quando a densidade tende a zero (Figura 3):
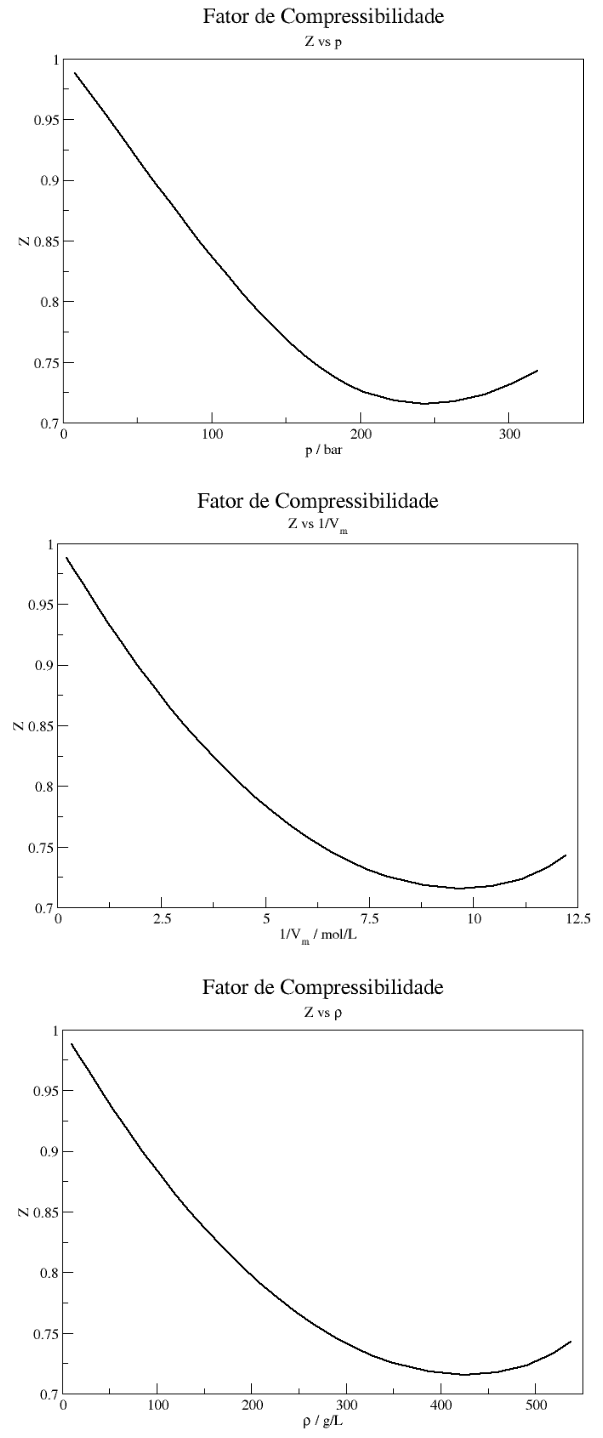
Figura 3. Fator de compressibilidade em função de pressão, recíproco do volume molar e densidade, a 150 °C, para N2O. Valores plotados foram obtidos a partir do trabalho de Couch & Kobe.1
As observações acima não dependem da natureza do gás estudado. Desta forma, podemos sumarizar que todos os gases se comportam idealmente quando essas condições experimentais são obedecidas. Matematicamente, temos:
Ajuste polinomial de Z
No entanto, esse valor de $Z$ só pode ser garantido em condições específicas. Como podemos descrever o valor de $Z$ para todas as faixas de pressão, volume molar ou densidade? Uma forma de se fazer isso é notando que as curvas apresentadas nas Figuras 1 e 2 podem ser reproduzidas através de polinômios de $Z$ em função da variável adequada ($p$, $V_m$ ou $\rho$, a depender do gráfico construído). Por exemplo, podemos o ajuste das curvas de $Z$ vs $p$ apresentadas na Figura 1 como polinômios em $p$ (Figura 4) fornecem:
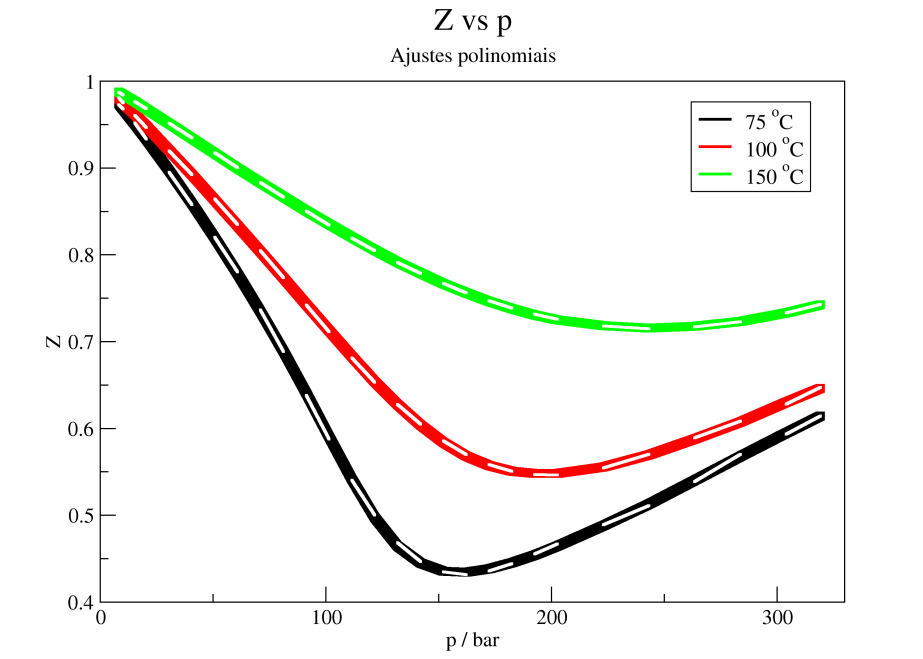
Figura 4. Gráfico de $Z$ vs $p$ para N2O, a temperaturas de 75, 100 e 150 °C. As linhas tracejadas em branco são os ajustes polinomiais de $Z$ em função de $p$ apresentados abaixo. Valores plotados foram obtidos a partir do trabalho de Couch & Kobe.1
As curvas tracejadas brancas na Figura 3 são os ajustes polinomiais de cada curva. Os coeficientes desses ajustes são os que seguem abaixo:
\[\small{Z(p; T = 150 ^{\circ}C) = 1,00 \:–\: 1,47 \times 10^{-3} \,p \:–\: 4,59 \times 10^{-6} \,p^2 \:+\: 3,37 \times 10^{-8} \,p^3 \:–\: 3,98 \times 10^{-11} \,p^4}\] \[\small{Z(p; T = 100 ^{\circ}C) = 1,00 \:–\: 2,77 \times 10^{-3} \,p \:+\: 1,42 \times 10^{-5} \,p^2 \:-\: 3,56 \times 10^{-7} \,p^3 \:+\: 2,80 \times 10^{-9} \,p^4 \\ -\: 8,23 \times 10^{-12} \,p^5 \:+\: 8,40 \times 10^{-15} \,p^6}\] \[\small{Z(p; T = 75 ^{\circ}C) = 1,00 \:–\: 2,02 \times 10^{-3} \,p \:-\: 1,43 \times 10^{-4} \,p^2 \:+\: 5,40 \times 10^{-6} \,p^3 \:-\: 1,00 \times 10^{-7} \,p^4 \\ +\: 9,85 \times 10^{-10} \,p^5 \:-\: 5,39 \times 10^{-12} \,p^6 \:-\: 1,67 \times 10^{-14} \,p^7 \:-\: 2,74 \times 10^{-17} \,p^8 \:+\: 1,86 \times 10^{-20} \,p^9}\]
Podemos notar que:
a) Os coeficientes dos polinômios diminuem, em módulo, com o grau de $p$. Por exemplo, para uma temperatura de 150 °C, vemos que |1,00| > |$-1,47 \times 10^{-3}$| > |$-4,59 \times 10^{-6}$| > $\cdots$ > |$-3,98 \times 10^{-11}$|. O mesmo vale para os coeficientes das outras temperaturas apresentadas;
b) Quanto mais distante da idealidade, mais termos no polinômio são necessários para reproduzir os dados experimentais. Para T = 75 °C, que apresenta o maior desvio da idealidade entre as três isotermas apresentadas, o polinômio é de grau 9. Já para T = 150 °C, o polinômio é de grau 4;
c) Ao compararmos o mesmo coeficiente para duas isotermas distintas, o módulo do coeficiente varia com a temperatura: no geral, ele aumenta quanto maior for o desvio de idealidade. Por exemplo, o coeficiente do termo em $p^2$ para T = 75 °C é, em módulo, $1,43 \times 10^{-4}$, mas para T = 150 °C é $4,59 \times 10^{-6}$.
Equações de estado de gases reais
A expansão do virial
Essa descrição polinomial de $Z$ em $p$ pode ser aplicada para $Z$ em função de $1/V_m$ ou de $\rho$. Para além disso, ela também pode ser aplicada para qualquer gás, pois os coeficientes dos polinômios irão depender (para além da tempeartura) da natureza do gás. Logo, podemos generalizar essa descrição utilizando o que chamamos de expansão do virial:
e os coeficientes destas equações ($\boldsymbol{B}$'s) são chamados de coeficientes do virial. Mais especificamente, dizemos que o termo $B_{2x}(T)$ é o segundo coeficiente do virial, $B_{3x}(T)$ é o terceiro coeficiente do virial, e assim por diante. Como visto nos gráficos, todos eles dependem exclusivamente da temperatura (e do gás avaliado). Dentre os coeficientes, o segundo é mais importante, por ser a primeira correção na descrição do desvio de idealidade de um gás. Existe uma temperatura na qual $B_{2x}(T)$ é zero, o que pode ser interpretado como um balanço entre as forças atrativas e repulsivas no gás. Essa temperatura é conhecida como temperatura de Boyle. Através da termodinâmica estatística, é possível atribuir um significado físico aos coeficientes do virial: os $B_{2x}(T)$'s estão relacionados às interações por pares; os $B_{3x}(T)$'s com as interações por trios de moléculas; os $B_{4x}(T)$'s com quartetos, e assim por diante.
Equação de van der Waals
Apesar de geral, a expansão do virial pode não ser prática de se trabalhar, por possuir muitos coeficientes que dependem da temperatura. Outras aproximações mais simples foram desenvolvidas para tentar descrever a relação entre as propriedades de estado de um gás imperfeito. Dentre elas, a mais célebre é, provavelmente, a equação de estado de van der Waals (vdW):
Esta equação introduz dois parâmetros que incorporam a especificidade molecular: o parâmetro “$a$”, relacionado à interação intermolecular, e o parâmetro “$b$”, relacionado ao volume molecular. Veremos adiante como essa equação pode ser obtida a partir de modelos teóricos. Ela, contudo, pode ser vista como uma equação efetiva, ou seja, um ajuste matemático simples a dados experimentais e como uma extensão da equação de estado dos gases ideais: caso ambos parâmetros de desvio de idealidade sejam iguais a zero (um gás ideal), então a equação dos gases ideais é recuperada. Tendo os valores de $a$ e $b$ para um determinado gás, é possível predizer valores de pressão em função do volume molar a uma dada temperatura, por exemplo.
É possível combinar a e.d.e. de v.d.W. com a equação do virial, para fornecer:
Equações de Redlich-Kwong e Peng-Robinson
A e.d.e. de vdW é muito simples - apenas dois termos constantes servem como parâmetro de especificidade molecular para descrever desvios de idealidade. Como era de se esperar, nem sempre a equação de vdW representa bem os dados experimentais. Assim, diversas outras equações de estado foram desenvolvidas ao longo do tempo, para capturar melhor os desvios de idealidade de gases reais. Outro exemplo é a e.d.e. de Redlich-Kwong (RK):
ou, ainda, a equação de Peng-Robinson (PR):
Para todas as e.d.e. acima (vdW, RK, PR), os parâmetros de especificidade molecular ($a$ e $b$, $A$ e $B$ ou $\alpha$ e $\beta$) são ajustados de forma a reproduzir os dados experimentais o melhor possível. Apesar de não possuírem fundamentação teórica, essas equações são capazes de reproduzir a relação efetiva entre variáveis de estado de fluidos, servindo para predição de propriedades em vários sistemas. Mostramos abaixo uma comparação entre a pressão determinada experimentalmente e utilizando as equações de vdW e de RK para N2O a 150 °C (Figura 5).
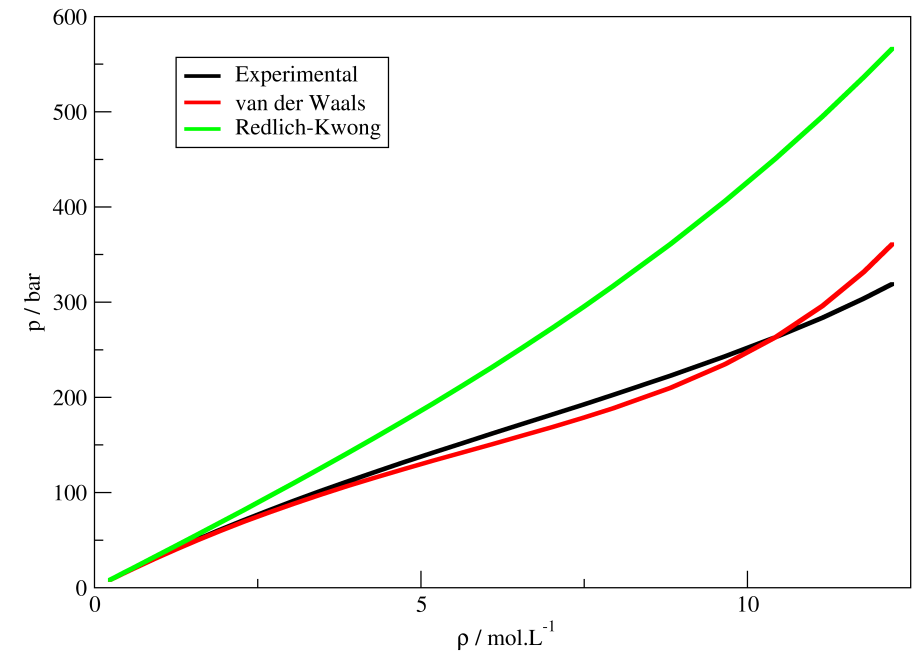
Figura 5. Comparação entre pressão experimental e calculadas pelas equações de van der Waals e Redlich-Kwong para N2O a 150 °C. Valores plotados foram obtidos a partir do trabalho de Couch & Kobe.1
Notamos que ambas equações reproduzem os valores a baixas densidades, mas o desvio do valor experimental aumenta com a densidade. Uma reprodução dos valores experimentais depende de da qualidade dos parâmetros utilizados e da temperatura. Contudo, as equações de vdW e de RK ainda são capazes de capturar algum desvio de idealidade – independente da temperatura e densidades utilizadas.
As e.d.e.'s, para além de permitirem calcularmos propriedades macroscópicas em função de variáveis e parâmetros, quando analisadas com mais profundidade, se mostram ainda mais gerais do que a primeira vista - elas não servem exclusivamente para gases. Veremos, a seguir, como é possível conectar os parâmetros dessas equações com propriedades experimentais.
1 Couch, E. J.; Kobe, K. A. Volumetric Behavior of Nitrous Oxide. Pressure-Volume Isotherms at High Pressures. J. Chem. Eng. Data 1961, 6 (2), 229–233. DOI: 10.1021/je60010a015.