A Termodinâmica pode ser definida como a área de estudo da relação entre energia, trabalho, calor e temperatura. Até agora, definimos a temperatura do ponto de vista microscópico, relacionando-a com a energia cinética média das moléculas do sistema (TC2.4). Ainda veremos outras definições para a temperatura, incluindo o ponto de vista da termodinâmica clássica. Antes disso, devemos definir mais rigorosamente o que são as outras quantidades: energia, trabalho e calor.
Trabalho termodinâmico é função de caminho
Pela mecânica clássica, o trabalho causado pelo deslocamento infinitesimal, $\vec {ds}$, de um corpo por ação de uma força, $\vec F$, é dado por:
e se os vetores possuem mesma direção e sentido, então a última igualdade é obtida (o termo $F_s$ enfatiza isso).
Essa força pode possuir duas origens distintas: a primeira são aquelas provenientes de potenciais, como por exemplo os de interação intermolecular. Essas forças podem ser definidas como o negativo do gradiente do potencial e são chamadas de forças conservativas. Por ora, não trataremos dessas forças, mas sim das pertencentes ao segundo grupo. O segundo grupo de forças é oriundo de forças externas, que não são originadas a partir de potenciais. Tais forças são chamadas de não conservativas, ou dissipativas. Para este segundo grupo de forças, o trabalho deverá ser escrito na forma:
sendo aqui $C$ o caminho específico tomado. Para que o trabalho seja calculado, é necessário saber o caminho tomado, pois a força varia ao longo do caminho. Assim, não existe um "trabalho inicial", nem um "trabalho final": trabalho é próprio processo. Isso faz com que a integração do lado esquerdo da equação TC7.2 não seja uma diferença, mas apenas $w$. Esse tipo de propriedade que depende de qual foi o caminho tomado é chamada de função de caminho, e o trabalho é um exemplo. O diferencial dessas quantidades será denotado por đ, neste curso - para indicar que o diferencial é inexato.
Trabalho de expansão/compressão
Existem diferentes formas de se realizar trabalho na termodinâmica, mas o mais simples de todos, é o trabalho de expansão/compressão de um gás. Vamos considerar um pistão com êmbolo móvel, sobre o qual uma força externa $F_{ext}$ está sendo exercida ao longo do eixo $s$, onde haverá deslocamento. Sabendo que esta se relaciona com a pressão externa ($p_{ext}$) e a área ($A$) sobre a qual a força está sendo exercida, podemos manipular a equação TC7.2 para obter:
pois o produto do deslocamento de altura do êmbolo no eixo s pela área do mesmo é a própria variação de volume do sistema. Em cursos de Química, no geral, o sinal negativo é colocado na frente da equação por uma questão de referencial. Compressões, que levam à diminuição do volume do sistema, fazem com que o trabalho seja positivo, pois a pressão é necessariamente positiva. Já expansões, que levam ao aumento do volume do sistema, são negativas. No primeiro caso, dizemos que trabalho foi realizado sobre o sistema. No segundo, dizemos que trabalho foi realizado pelo sistema.
A expressão para o trabalho em TC7.3 foi modificada para trabalharmos com as variáveis mais práticas em sistemas gasos. Contudo, ela continua sendo uma expressão que depende do caminho tomado. O problema é que a quantidade de caminhos possíveis entre um estado inicial e um final é incontável. Assim, vamos nos concentrar nos três caminhos mais comuns/simples.
Expansão contra o vácuo - expansão livre
Vamos considerar um sistema composto por dois subsistemas, separados por uma parede impermeável. No subsistema 1, há um gás ideal, ocupando um certo volume inicial, a uma certa pressão e temperatura. No subsistema 2 há apenas vácuo. Agora, vamos imaginar que há um dispositivo que pode ser disparado e ele abrirá uma passagem entre os dois subsistemas, permitindo a passagem de matéria entre os subsistemas. O que esperamos neste caso é que o gás, antes confinado apenas no subsistema 1, se expanda espontaneamente, isto é, sem que seja necessária nenhuma ação externa para que o evento ocorra, e ocupe ambos os subsistemas. Ao final do processo, o gás estará em um estado de equilíbrio, ocupando um volume maior e com uma pressão menor. Entretanto, por ser um gás ideal, a temperatura será a mesma. Qual foi o trabalho realizado no processo? Como a pressão externa era zero durante a expansão:
e essa expansão ocorre sem que trabalho seja realizado.
Expansão/compressão contra pressão constante
Vamos imaginar, agora, um processo de expansão/compressão no qual a pressão externa é mantida constante durante o processo. Se o volume inicial é $V_i$ e o volume final é $V_f$, então o trabalho será:
Algumas observações quanto ao que foi obtido. Notamos que o termo $B_{2V}(T)$ tem origem na inclusão de interações por pares de moléculas. Veremos adiante que, quando trios, quartetos e etc são incluídos no modelo, os outros termos do virial aparecem. O coeficiente $B_{2V}(T)$ depende exclusivamente da temperatura (e da natureza das moléculas interagindo), como observado experimentalmente. Se o potencial de interação for zero, então B2V(T) = 0 e $Z = 1$, ou seja, um gás ideal. Por fim, utilizaremos a equação TC5.4 na elaboração de modelos moleculares que possam explicar o desvio de idealidade em sistemas gasos – i.e., caso a forma de $u(r)$ seja definida, é possível determinar $B_{2V}(T)$ e, porseguinte, escrever uma e.d.e. para o modelo de gás em questão.
O modelo de esferas rígidas não interagentes
Vamos iniciar nossos estudos com modelos simples e introduzir complexidade a eles. Dos modelos de gases reais, o mais simples de todos é o modelo de esferas rígidas. Neste modelo, as moléculas são esféricas, possuindo um diâmetro $\sigma$, e são impenetráveis. Matematicamente, podemos definir o potencial de interação dessas moléculas na forma:
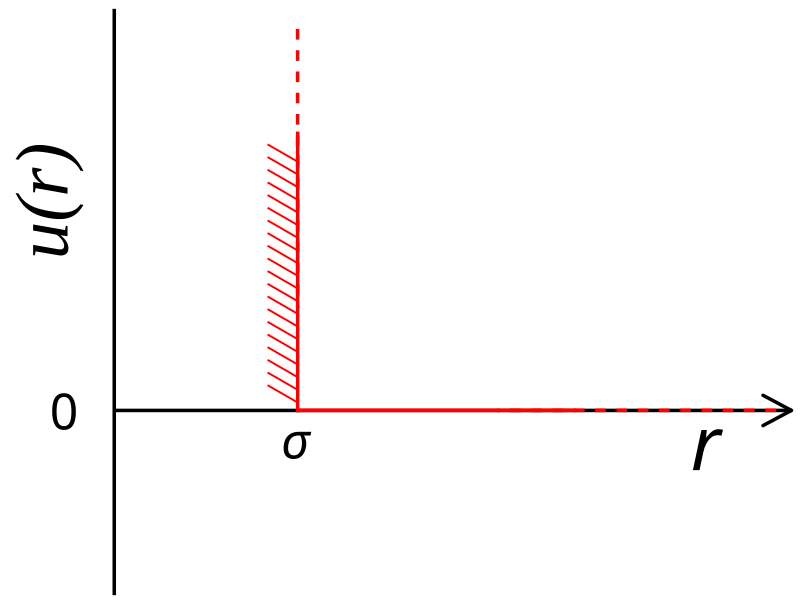
E a figura da direita representa o potencial dessa esfera rígida. É interessante notar que o tamanho da molécula surge por conta de um potencial repulsivo. Não é possível duas moléculas dessa espécie se aproximarem mais do que o diâmetro delas, mas elas não interagem para nenhuma outra distância. Agora, podemos utilizar a equação substituir esse potencial na equação TC5.4. Contudo, por ser um potencial descontínuo, devemos integrar em duas regiões: uma com $0 \le r \lt \sigma$ e outra com $r \ge \sigma$. Como o potencial é zero no segundo trecho de integração, a segunda integral será zero e:
E, como desejado, obtivemos uma expressão para o segundo coeficiente do virial. Notamos que essa expressão para $B_{2V}$ é independente da temperatura - apenas uma constante, $b$, que está relacionada com o volume da molécula. Em seguida, podemos utilizar a expressão obtida em TC5.6 na expressão do virial (TC5.3) e escrever uma nova e.d.e. para esse modelo de molécula:
e a última linha foi obtida considerando que $b \ll \bar V$, permitindo a transformação utilizando a série de Maclaurin $1+\frac{b}{\bar V} \approx \frac{1}{1-\bar V}$.
Esse primeiro modelo, de esferas rígidas, mostra que o potencial intermolecular pode mudar, de fato, a e.d.e. de um gás. Este gás não é mais um GI, por possuir tamanho finito. Logo, a sua e.d.e. já não é a de um GI, também. Vale a pena notar também que, caso tomemos $\lim_{\sigma \ to 0} B_{2V} = 0$ e voltaremos a ter um gás ideal - que é o esperado, pois a molécula não possui tamanho - é puntiforme - novamente. Percebam que nenhum termo de interação atrativa foi adicionado - apenas um repulsivo, relacionado ao tamanho da molécula. O que devemos esperar da e.d.e. de um gás com parte atrativa no potencial intermolecular?
O potencial de poço quadrado
Um outro modelo muito simples com potencial atrativo é o modelo das esferas rígidas com um potencial atrativo quadrado. Similar às esferas rígidas, esse potencial é descontínuo e possui 3 regiões: uma de esfera rígida, outra de potencial constante e negativo, e outra com potencial igual a zero:
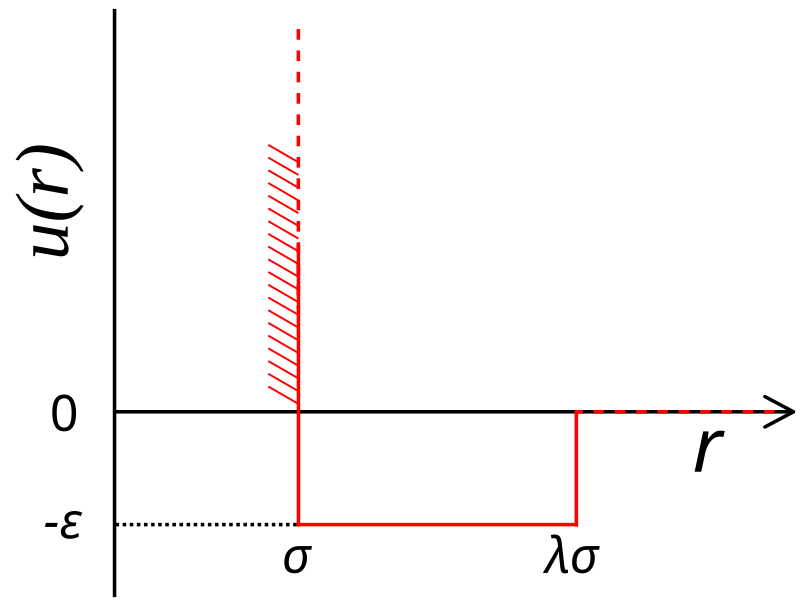
Aqui, o parâmetro $\lambda$ determina a espessura desse poço de potencial negativo - quanto maior o seu valor, maior é o alcance da interação -, enquanto o parâmetro $\varepsilon$ é a profundidade desse potencial - quanto maior o seu valor, mais forte é a interação intermolecular. Devemos notar que, caso façamos $\lambda=1$, então $\varepsilon=0$, necessariamente, e obtemos de volta o potencial de esferas rígidas. Caso façamos o mesmo procedimento realizado para as esferas rígidas, obteremos um $B_{2V}(T)$ e uma nova e.d.e. pode ser escrita:
Esse coeficiente, diferentemente do modelo anterior, possui dependência com a temperatura através do termo $e^{\beta\varepsilon}$. Como $\varepsilon$ é positivo, então o valor de $B_{2V}(T)$ aumenta com a profundidade do poço. Esse resultado é esperado: quanto maior for a interação intermolecular, maior deverá ser o desvio da idealidade. Além disso, quando a temperatura aumenta, o valor de $B_{2V}(T)$ diminui. Isto ocorre porque as interações intermoleculares ficam menos relevantes quando comparadas à energia térmica, $RT$. Também, como esperado, se $\lambda = 1$, então $B_{2V} = b$, o coeficiente para uma esfera rígida. Um bom avanço neste modelo é o surgimento da dependência de $B_{2V}$ com a temperatura - algo ausente nas esferas rígidas.
Esfera rígida de London
Um problema do potencial anterior é que o potencial atrativo é simples demais - nenhum átomo ou molécula conhecidos possuem um potencial de interação quadrado. Logo após o desenvolvimento da mecânica quântica, London utilizou-se dela para fornecer um modelo teórico para a atração entre moléculas de gases nobres. Segundo sua teoria, o potencial atrativo entre os gases nobres deveria ser do tipo $u(r) \propto -1/r^6$, sendo $r$ a distância entre as moléculas. Esse termo sozinho, entretanto, daria origem a um colapso - as moléculas deveriam se encontrar com os seus núcleos uns sobre os outros, pois esta seria a configuração de menor energia. O termo repulsivo é mais complicado de se modelar, então vamos imaginar uma esfera rígida que possui uma parte atrativa segundo o potencial de London:
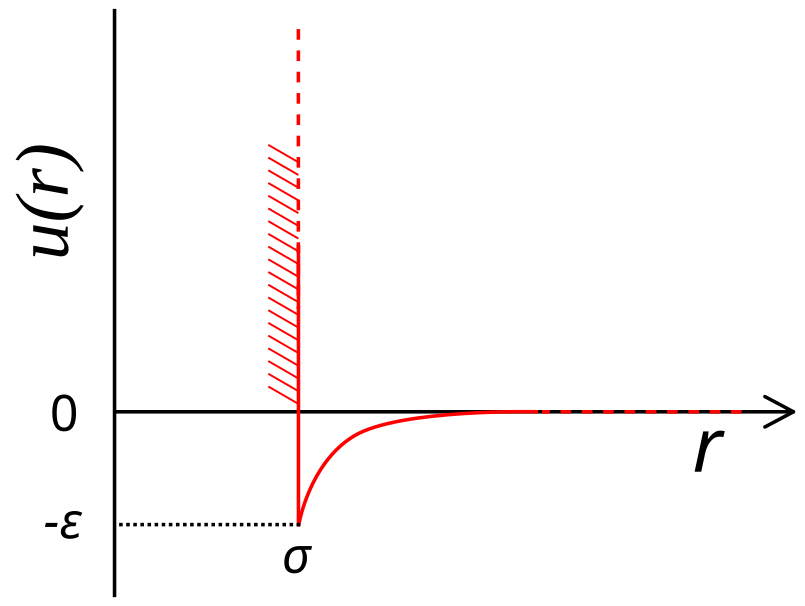
sendo $\sigma$ o diâmetro molecular e $\varepsilon$ é a profundidade do potencial quando $r \to \sigma$. Esse potencial aprimora o modelo anterior por utilizar um potencial atrativo que possui fundamentação teórica e que depende da distância intermolecular. No entatno, este potencial também é descontínuo.
As integrais com esse potencial podem ser mais trabalhosas de se resolver. Contudo, se utilizarmos o limite termodinâmico, isto é, $\frac{u(r)}{k_B T} \ll 1$. O desenvolvimento da metodologia aplicada para os modelos anteriores fornece:
Quando comparamos a equação TC5.11b com a equação TC3.4b, vemos que o termo $B_{2V}(T)$ é o mesmo em ambas equações. Ou seja, o modelo de esfera rígida de London é o modelo que dá origem à equação de estado de van der Waals! Revisitaremos esse modelo na parte de Termodinâmica estatística.
Potencial de Lennard-Jones
Por último, temos o potencial de Lennard-Jones. Este potencial utiliza o termo repulsivo de London, mas usa um termo atrativo na forma $u(r) \propto \frac{1}{r^6}$, fazendo deste potencial contínuo para todos os valores de $r$. O potencial é o seguinte:
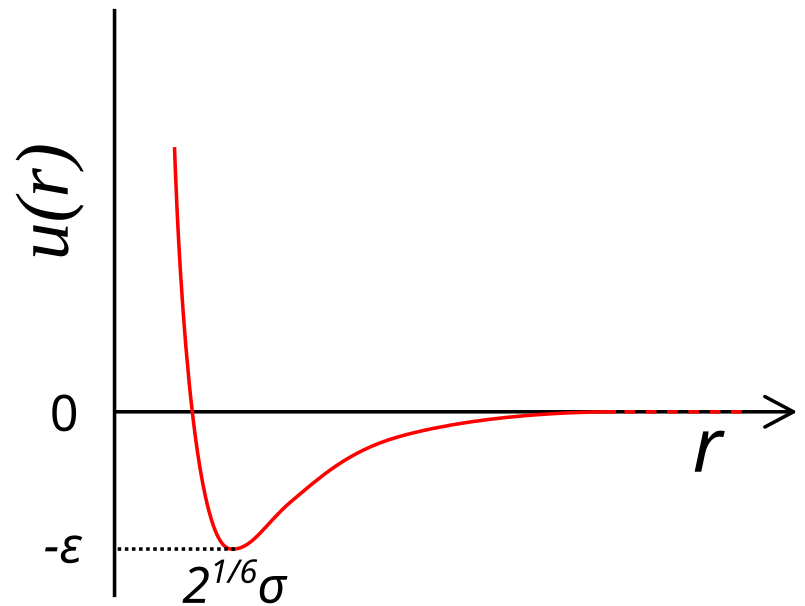
Este potencial diverge para $r \to 0$ e converge para $r \to \infty$, possuindo ainda um mínimo. Ele, contudo, não pode ser avaliado analiticamente, como fizemos até então. No entanto, ele pode (e é) amplamente utilizado em métodos computacionais clássicos de simulação molecular.
Agora que as equações de estado de gases estão bem definidas, estamos prontos para iniciar a discussão sobre as leis fundamentais da termodinâmica.