Modelando desvios de idealidade
Como vimos, as equações de estado de gases reais têm como objetivo capturar a relação real entre as variáveis do conjunto completo para gases que não se comportam idealmente. Também vimos que esse desvio possui duas raízes: gases reais não são puntiformes, i.e., eles ocupam um volume no espaço, e as moléculas podem interagir umas com as outras, dando origem às interações intermoleculares. Agora, vamos ver que é possível relacionar os parâmetros dessas equações com essas propriedades moleculares – tamanho e capacidade de interagir com outras moléculas.
Desvio de idealidade surge de interações intermoleculares
Uma forma possível de se fazer isso é através do teorema do virial. No desenvolvimento inicial (TC2.1), consideramos um sistema composto por $N$ moléculas e que a força exercida por um átomo sobre os outros seria zero, fazendo com que a equação tivesse apenas dois termos – um de energia cinética e outro de colisão com as paredes do recipiente. Agora, vamos considerar um sistema formado por $N$ moléculas esféricas (sem estrutura interna) idênticas, no qual as interações intermoleculares estão presentes, mas apenas na forma de interações radiais aditivas por pares – isto é, a força total exercida na molécula $i$ pelas outras $j \ne i$ moléculas do sistema é dada pela soma de $N – 1$ forças oriundas do potencial de interação radial por pares. Graças a essas propriedades, podemos definir que $\vec F_{i,j} = -\vec F_{j,i}$, i.e., a força exercida na molécula $i$ pela molécula $j$ é igual ao oposto da força exercida na molécula $j$ pela molécula $i$. Caso definamos o vetor distância entre a molécula $i$ e a molécula $j$ na forma , então podemos manipular a equação TC2.1 para obter:
E qual é o significado físico do último termo em TC5.1? Ele é a média sobre todo o sistema do produto escalar entre os vetores força e distância entre as moléculas $i$ e $j$. No caso de gases ideais, a força de interação é zero e esse termo de interação não existe, levando à equação dos gases ideais. Em outras palavras, isso significa que, para um gás ideal, se olharmos para uma molécula em particular e determinarmos a densidade de moléculas ao redor dela em uma casca esférica de raios $r$ e $r + dr$, essa densidade de moléculas deve ser independente da distância $r$ e da espessura $dr$ da casca, uma vez que não há interação intermolecular entre as partículas e a molécula central é puntiforme.
Obtendo o termo de não idealidade
Contudo, para moléculas interagentes e de volume finito, pode haver uma distância ótima de interação, fazendo com que haja excesso de moléculas nessa distância – ou regiões com depleção de moléculas, dependendo das interações intermoleculares, da densidade de moléculas e do empacotamento delas. Voltando ao último termo de TC5.1, como podemos calculá-lo para moléculas interagentes e finitas? É possível fazer isso assumindo algumas coisas:
1. Todas as $N$ moléculas do sistema são idênticas e não possuem estrutura interna;
2. Para um sistema isotrópico, a média do produto escalar $\vec F_{i,j} \cdot \vec r_i$ deve ser igual à média do produto para qualquer par de moléculas;
3. O número total de interações possíveis no sistema pode ser calculado pela combinação de $N$ moléculas tomadas duas a duas;
4. $N$ é da ordem do número de Avogadro ($N_A$, $\approx$ $6,022 \times 10^{23}$), fazendo com que as médias possam ser tomadas a partir da distribuição de Boltzmann (veremos isso mais adiante);
5. Os vetores força e distância entre as moléculas i e j possuem mesma direção e sentido, então o produto escalar entre eles é o produto de seus módulos;
6. As forças intermoleculares são oriundas do potencial intermolecular [$u(\vec r_{i,j})$]entre as moléculas, isto é $\vec F(r_{i,j}) = \frac{du}{r_{i,j}} \hat r_{i,j}$;
7. A densidade do gás é relativamente baixa;
8. A O vetor $\vec r_{i,j}$ pode ser transformado no escalar $r$ fixando uma das partículas na origem do sistema e utilizando coordenadas esféricas polares;
9. O potencial de interação intermolecular, $u$, é consideravelmente menor que a energia térmica, $k_BT$;
10. Esse potencial deve ser convergente para distâncias infinitas, com formas do tipo $u(r_{i,j}) \propto -\frac{1}{r^n}$.
Caso essas condições acima sejam satisfeitas/consideradas, o último termo da equação TC5.1 pode ser reescrito na forma:
sendo $r$ a distância entre duas moléculas e $\beta = \frac{1}{k_BT}$. Vimos que esse termo surge pela interação entre pares de partículas, ou seja, é um termo de desvio de idealidade. De fato, se o potencial de interação entre as partículas for igual a zero, o termo dentro da integral do lado direito em TC5.2 será igual a zero, zerando o termo como um todo, fazendo com que TC5.1 seja, novamente, a e.d.e. de um gás ideal.
Teorema do virial e o coeficiente $B_{2V}(T)$
Vamos, agora, substituir esse termo de interação intermolecular no teorema do virial e, fazendo algumas manipulações, relacionar a equação final com o fator de compressibilidade, $Z$:
E, na última linha, utilizamos o fato de saber que o fator de compressibilidade pode ser escrito como uma função polinomial em $\frac{1}{\bar V}$, e que o segundo coeficiente do virial é maior em módulo do que o terceiro e assim por diante. Então, considerando o fator de compressibilidade como um polinômio truncado no termo em $\frac{1}{\bar V}$, definimos o segundo coeficiente do viral na forma:
Algumas observações quanto ao que foi obtido. Notamos que o termo $B_{2V}(T)$ tem origem na inclusão de interações por pares de moléculas. Veremos adiante que, quando trios, quartetos e etc são incluídos no modelo, os outros termos do virial aparecem. O coeficiente $B_{2V}(T)$ depende exclusivamente da temperatura (e da natureza das moléculas interagindo), como observado experimentalmente. Se o potencial de interação for zero, então B2V(T) = 0 e $Z = 1$, ou seja, um gás ideal. Por fim, utilizaremos a equação TC5.4 na elaboração de modelos moleculares que possam explicar o desvio de idealidade em sistemas gasos – i.e., caso a forma de $u(r)$ seja definida, é possível determinar $B_{2V}(T)$ e, porseguinte, escrever uma e.d.e. para o modelo de gás em questão.
O modelo de esferas rígidas sem atração
Vamos iniciar nossos estudos com modelos simples e introduzir complexidade conforme avançarmos. Dos modelos de gases reais, o mais simples de todos é o modelo de esferas rígidas. Neste modelo, as moléculas são esféricas, possuindo um diâmetro $\sigma$, e são impenetráveis. Matematicamente, podemos definir o potencial de interação dessas moléculas na forma:
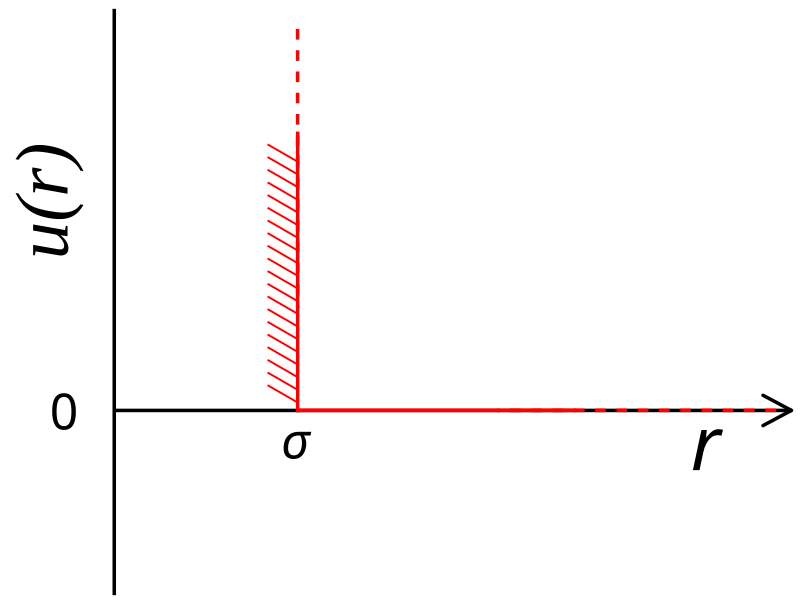
E a figura da direita representa o potencial dessa esfera rígida. É interessante notar que o tamanho da molécula surge por conta de um potencial repulsivo. Não é possível duas moléculas dessa espécie se aproximarem mais do que o diâmetro delas, mas elas não interagem para nenhuma outra distância. Agora, podemos utilizar a equação substituir esse potencial na equação TC5.4. Contudo, por ser um potencial descontínuo, devemos integrar em duas regiões: uma com $0 \le r \lt \sigma$ e outra com $r \ge \sigma$. Como o potencial é zero no segundo trecho de integração, a segunda integral será zero e:
E, como desejado, obtivemos uma expressão para o segundo coeficiente do virial. Notamos que essa expressão para $B_{2V}$ é independente da temperatura - apenas uma constante, $b$, que está relacionada com o volume da molécula. Em seguida, podemos utilizar a expressão obtida em TC5.6 na expressão do virial (TC5.3) e escrever uma nova e.d.e. para esse modelo de molécula:
e a última linha foi obtida considerando que $b \ll \bar V$, permitindo a transformação utilizando a série de Maclaurin $1+\frac{b}{\bar V} \approx \frac{\bar V}{\bar V - b}$.
Esse primeiro modelo, de esferas rígidas, mostra que o potencial intermolecular pode mudar, de fato, a e.d.e. de um gás. Este gás não é mais um GI, por possuir tamanho finito. Logo, a sua e.d.e. já não é a de um GI, também. Vale a pena notar também que, caso tomemos $\lim\limits_{\sigma \to 0} B_{2V} = 0$ e voltaremos a ter um gás ideal - que é o esperado, pois a molécula voltará a não possuir tamanho. Percebam que nenhum termo de interação atrativa foi adicionado - apenas um repulsivo, relacionado ao tamanho da molécula. O que devemos esperar da e.d.e. de um gás com parte atrativa no potencial intermolecular?
O potencial de poço quadrado
Um outro modelo muito simples com potencial atrativo é o modelo das esferas rígidas com um potencial atrativo quadrado. Similar às esferas rígidas, esse potencial é descontínuo e possui 3 regiões: uma de esfera rígida, outra de potencial constante e negativo, e outra com potencial igual a zero:
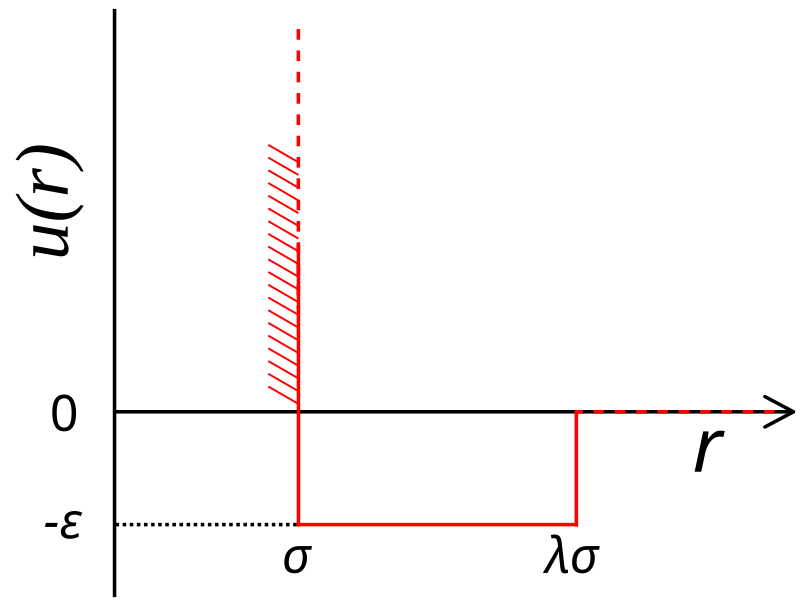
Aqui, o parâmetro $\lambda$ determina a espessura desse poço de potencial negativo - quanto maior o seu valor, maior é o alcance da interação -, enquanto o parâmetro $\varepsilon$ é a profundidade desse potencial - quanto maior o seu valor, mais forte é a interação intermolecular. Devemos notar que, caso façamos $\lambda=1$, então $\varepsilon=0$, necessariamente, e obtemos de volta o potencial de esferas rígidas. Caso façamos o mesmo procedimento realizado para as esferas rígidas, obteremos um $B_{2V}(T)$ e uma nova e.d.e. pode ser escrita:
Esse coeficiente, diferentemente do modelo anterior, possui dependência com a temperatura através do termo $e^{\beta\varepsilon}$. Como $\varepsilon$ é positivo, então o valor de $B_{2V}(T)$ aumenta com a profundidade do poço. Esse resultado é esperado: quanto maior for a interação intermolecular, maior deverá ser o desvio da idealidade. Além disso, quando a temperatura aumenta, o valor de $B_{2V}(T)$ diminui. Isto ocorre porque as interações intermoleculares ficam menos relevantes quando comparadas à energia térmica, $RT$. Também, como esperado, se $\lambda = 1$, então $B_{2V} = b$, o coeficiente para uma esfera rígida. Um bom avanço neste modelo é o surgimento da dependência de $B_{2V}$ com a temperatura - algo ausente nas esferas rígidas.
Esfera rígida de London
Um problema do potencial anterior é que o potencial atrativo é simples demais - nenhum átomo ou molécula conhecidos possuem um potencial de interação quadrado. Logo após o desenvolvimento da mecânica quântica, London utilizou-se dela para fornecer um modelo teórico para a atração entre moléculas de gases nobres. Segundo sua teoria, o potencial atrativo entre os gases nobres deveria ser do tipo $u(r) \propto -1/r^6$, sendo $r$ a distância entre as moléculas. Esse termo sozinho, entretanto, daria origem a um colapso - as moléculas deveriam se encontrar com os seus núcleos uns sobre os outros, pois esta seria a configuração de menor energia. O termo repulsivo é mais complicado de se modelar, então vamos imaginar uma esfera rígida que possui uma parte atrativa segundo o potencial de London:
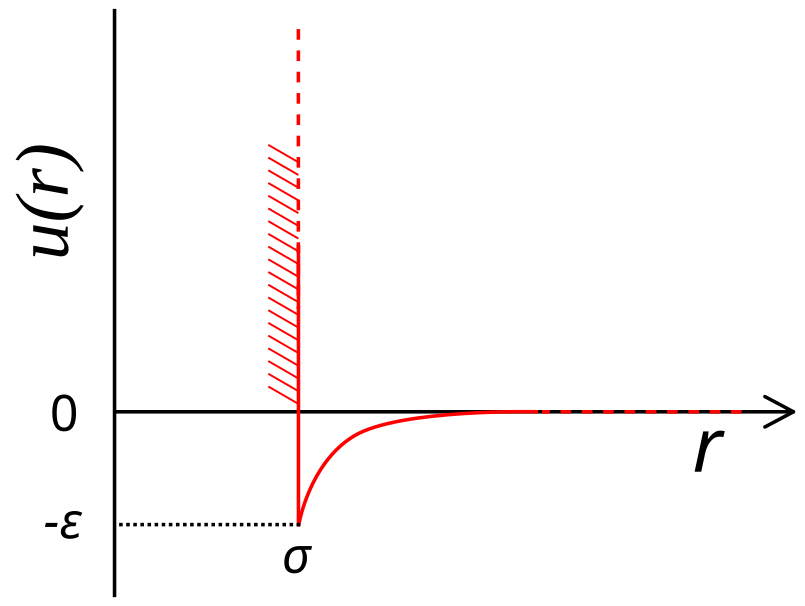
sendo $\sigma$ o diâmetro molecular e $\varepsilon$ é a profundidade do potencial quando $r \to \sigma$. Esse potencial aprimora o modelo anterior por utilizar um potencial atrativo que possui fundamentação teórica e que depende da distância intermolecular. No entatno, este potencial também é descontínuo.
As integrais com esse potencial podem ser mais trabalhosas de se resolver. Contudo, se utilizarmos o limite termodinâmico, isto é, $\frac{u(r)}{k_B T} \ll 1$. O desenvolvimento da metodologia aplicada para os modelos anteriores fornece:
Quando comparamos a equação TC5.11b com a equação TC3.4b, vemos que o termo $B_{2V}(T)$ é o mesmo em ambas equações. Ou seja, o modelo de esfera rígida de London é o modelo que dá origem à equação de estado de van der Waals! Revisitaremos esse modelo na parte de Termodinâmica estatística.
Potencial de Lennard-Jones
Por último, temos o potencial de Lennard-Jones. Este potencial utiliza o termo repulsivo de London, mas usa um termo atrativo na forma $u(r) \propto \frac{1}{r^6}$, fazendo deste potencial contínuo para todos os valores de $r$. O potencial é o seguinte:
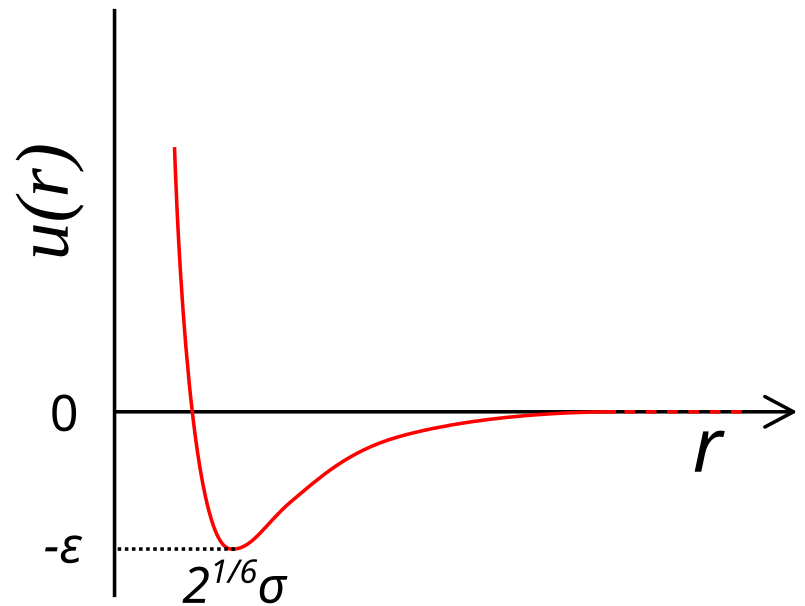
Este potencial diverge para $r \to 0$ e converge para $r \to \infty$, possuindo ainda um mínimo. Ele, contudo, não pode ser avaliado analiticamente, como fizemos até então. No entanto, ele pode (e é) amplamente utilizado em métodos computacionais clássicos de simulação molecular.
Agora que as equações de estado de gases estão bem definidas, estamos prontos para iniciar a discussão sobre as leis fundamentais da termodinâmica.